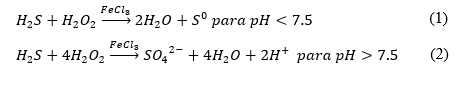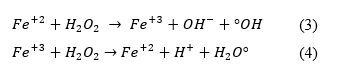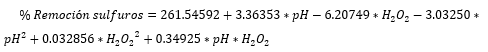|
Aplicación de foto fenton (VIS) para la remoción de sulfuros y DQO en aguas residuales de curtiembre
Rafael Nikolay Agudelo Valencia1
Recibido: 18 julio 2019 Aceptado: 16 junio 2019 Actualizado: 17 diciembre 2019
DOI: DOI: 10.17151/luaz.2020.50.11
Resumen
La producción de cueros se constituye como una actividad de vital importancia económica, social y cultural. Sin embargo, la calidad de los cuerpos de agua en los cuales son vertidas las aguas residuales procedentes de esta industria se ven afectados por el aporte de carga contaminante. Objetivo: demostrar la reducción en la concentración de sulfuros y DQO evaluando las condiciones físicas y químicas del agua de curtiembre sin tratamiento, clarificada y tratada. Materiales y métodos: se propone un proceso de oxidación de avanzada, mediante la adición de peróxido de hidrógeno y cloruro férrico como catalizador (reactivo de Fenton), utilizando lámparas LED de luz visible como fuente de energía para la fotólisis de los contaminantes, el diseño experimental se realizó con tiempos de reacción fijo de seis horas, se analizó el efecto del pH y la dosis de peróxido (H2O2 y FeCl3) y como superficie de respuesta se obtuvo porcentaje de remoción en términos de sulfuros y DQO. Resultados: Se obtuvo una remoción de 73,5% para sulfuros en condiciones de pH inicial de solución de 5 y dosis de H2O2 al 30% de 40µl, y 56% de remoción de DQO para un pH inicial de 6 con dosis de H2O2 al 30% de 60µl, aunque se evidencia que las variables de respuesta dependen o varían respecto a las variables o factores de proceso según los resultados estadísticos de la ANOVA. Conclusiones: se alcanza mayor porcentaje de remoción de sulfuros cuando el pH inicial se encuentra entre cinco y seis unidades, mientras que la remoción de DQO depende de la concentración de H2O2 aplicada, además, el uso de radiación visible suministrada por lámparas LED para intensificar el proceso de oxidación resulta favorable de acuerdo con el análisis estequiométrico realizado de conformidad con la dosis de agente oxidante empleado.
Palabras clave: DQO, industria, radiación, sulfuro de hidrógeno, tratamiento de aguas residuales.
Applicability of photo-fenton process (visible-light) in the degradation of sulfur and cod from tannery wastewater
Abstract
Leather production is constituted as an activity of central importance, not only for the economy but for a social and cultural meaning, however, the quality of the waterbodies in which is poured the wastewater proceeded from this industry is affected by the high amount of pollutant load. Objective: decrease the level of concentration of sulfurs and COD, evaluating physical and chemical conditions of the tannery wastewater without treatment, clarified and treated. Materials and methods: an advanced oxidation process is proposed for the degradation of these substances, dosing peroxide of hydrogen and ferric chloride as catalyst (Fenton's reagent) in the presence of LED lamps of visible light as source of energy for the pollutant’s photolysis. The experimental design was realized for a reaction time of 6 hours, there was analyzed the effect of the pH and the dose of peroxide (H2O2 and FeCl3) and the responses surfaces were percentage of sulfur and DQO removal from wastewater treatment. Results: It was obtained an optimal removal of 73,5 % for sulfurs in conditions of initial solution pH of 5 and dose of H2O2 of 40µl and 56 % of COD´s removal for an initial pH of 6 with applied dose of H2O2 of 60µl, although it is remarkable that the response variables depend and change in relation to the processes’ factors according the ANOVA statistics results. Conclusion: For sulfur removal the best results are obtained when the initial pH value range between 5 and 6 units, while for COD, the removal percentage depends on the H2O2 applied doses, besides, the use of visible radiation supplied by LED lamps to intensify the oxidation process turns out favorable according with the stoichiometrical analysis.
Key words: COD, industry, radiation, sulfur, wastewater treatment.
Introducción
A 40 km de la capital y 6 km del nacimiento del río Bogotá están ubicados los municipios de Villapinzón y Chocontá; en el corredor vial que une a estos municipios, se conoce la presencia de aproximadamente 110 empresas dedicadas al curtido de pieles bovinas (Artuz, Martínez & Morales, 2011). Algunas de ellas con carencia de un tratamiento de aguas residuales efectivo. Estas industrias proveen de empleo aproximadamente al 60% de la mano de obra disponible en la región. La mayoría son de tipo familiar y algunas se han mantenido por más de 120 años en la zona, de modo que esta actividad erige una tradición que contribuye al progreso económico de la región (UNAL, 2014).
El curtido es el proceso mediante el cual las pieles de animales son transformadas en cuero, el cual es empleado para la fabricación de distintos artículos, tales como bolsos, zapatos, chaquetas entre otros (Saxena, Rajoriya, Saharan & George, 2018). El procesamiento de cueros implica una serie de operaciones unitarias como son por ejemplo el remojo, el pelambre, desencalado, curtido, recurtido, teñido, entre otras. Estas operaciones generan una cantidad considerable de agua residual (Vilardi, Rodriguez-Rodriguez, Ochando Pulido, Verdone & Di Palma, 2018). En este sentido, dicho sector industrial es considerado como uno de los que mayor contaminación aporta en términos de complejidad de sus efluentes (Deghles & Kurt, 2016). Estos se caracterizan por presentar pH variable pasando por pH superiores a once unidades en las operaciones de pelambre o menores a cuareo en el piquelado de la piel, así como alta concentración de sólidos suspendidos (840 Kg/Ton piel), DQO (1042 Kg7Ton piel), sulfuros (87 Kg/Ton piel), cromo (3.3 Kg/Ton piel) y cloruros (412 Kg/Ton piel) (Aboulhassan, Souabi & Yaacoubi, 2008). La etapa de pelambre o depilado representa la mayor complejidad para el tratamiento debido al contenido de cal, sulfuro de sodio y materia orgánica expresada en altos valores de concentración de DQO, DBO y sólidos suspendidos (Jian, Wenyi & Wuyong, 2011).
El tratamiento de aguas residuales de curtimbres ha sido objeto de múltiples investigaciones, en las cuales se ha hecho uso de diversas tecnologías para la reducción de contaminantes. Dentro de las distintas alternativas evaluadas se pueden mencionar la coagulación química (Bajza, Hitrec & Muic, 2005), ósmosis inversa (Suthanthararajan et al., 2004), nano filtración (Cuartas-Uribe et al., 2006), oxidación con el reactivo de fenton y la combinación H2O2/UV (Schrank, José, Moreira & Schröder, 2005), biodegradación (Ganesh, Balaji & Ramanujam, 2006), entre otros. Con respecto a los tipos de tratamiento mencionados, la oxidación avanzada representa una de las tecnologías con mayor efectividad por la generación de radicales hidroxilo capaces de mineralizar múltiples sustancias (Andreozzi, Caprio, Insola & Marotta, 1999). La oxidación avanzada es un proceso en el cual no se presenta generación de lodos o residuos adicionales. En los procesos de oxidación avanzada se puede hacer uso de agentes oxidantes tales como el ozono y el peróxido de hidrógeno con catalizadores, además de la combinación con exposición a radiación UV o luz visible (Nivya & Pieus, 2016). Esta investigación tiene como objetivo demostrar la reducción en la concentración de sulfuros y DQO, evaluando condiciones físicas y químicas del agua de residual de curtiembre clarificada empleando métodos de oxidación avanzada que no han sido previamente empleados en las aguas residuales del sector curtiembres de Colombia; asimismo, evaluar la dosis de los agentes oxidantes en relación con cada contaminante.
Materiales y métodos
El agua residual empleada para la realización de los ensayos fue suministrada por una empresa de curtido de pieles bovinas ubicada en el municipio de Chocontá, Cundinamarca. La muestra de agua fue recolectada de acuerdo con el protocolo establecido por el IDEAM (Instituto de Hidrología, 2007). Posteriormente, la muestra fue caracterizada al inicio del proceso para determinar los valores de pH, conductividad (µS), turbidez (NTU), DQO (mg/L) y sulfuros (mgS2-/L); la cuantificación de cada uno de los parámetros se llevó a cabo siguiendo los métodos estándar para análisis de agua potable y residual (APHA; AWWA;WPC, 1995). El pH, la conductividad y la turbidez en campo fueron analizados con un multiparámetro marca Horiba U-50.
El agua residual fue clarificada con sulfato de aluminio (Al₂(SO₄)₃ 14H2O), a fin de remover la mayor cantidad de sólidos presentes y asegurar la penetración de la radiación visible dentro del líquido para intensificar el proceso de oxidación (Schrank et al., 2005). El diseño experimental tuvo como objeto determinar el efecto del pH inicial del agua residual y la dosis de peróxido de hidrógeno sobre la remoción de sulfuros y DQO, para lo cual se empleó un diseño experimental de tipo central compuesto, con dos factores en dos niveles y cinco réplicas del punto central, para un total de trece ensayos; las variables experimentales o factores fueron el pH inicial del agua residual clarificada (valores de 5 y 7) y la dosis de peróxido de hidrógeno al 30% (40 y 80 µL, equivalentes a 0.00702 y 0.01405 mmol). La temperatura del agua, la velocidad de agitación y el tiempo de reacción fueron mantenidos constantes con el objeto de solo analizar el efecto de las variables o factores seleccionados sobre las variables de respuesta. Se empleó el análisis de varianza de los resultados experimentales para analizar el efecto de los factores sobre los porcentajes de remoción y se utilizó la metodología denominada superficie de respuesta (SR) para presentar de manera gráfica el efecto de los factores sobre las variables de respuesta y hallar los valores de los factores analizados para los cuales se alcanzan las máximas remociones.
Para afirmar que los efectos de los factores contribuyen a explicar el comportamiento de la respuesta, se debe hacer la prueba estadística del análisis de varianza (ANOVA) (Gutiérrez Pulido & De la Vara Salazar, 2012). Se establece como hipótesis nula para el ANOVA que el pH inicial y la dosis de peróxido no afectan el porcentaje de remoción de sulfuros y DQO.
El pH inicial del agua fue ajustado con HCl 1 N y NaOH 1 N (Merk Millipore); la determinación de pH en laboratorio fue hecha con un potenciómetro Metrohm pH/Ion meter 780. Para realizar el proceso de oxidación avanzada se efectuó un montaje de laboratorio, en el cual se emplearon vasos de precipitado de 100 mL para cada una de las pruebas, una plancha de agitación tipo AREX, agitadores magnéticos universales, lámpara de luz led en el rango de radiación visible (450nm – 1 W), peróxido de hidrógeno (H2O2) al 30% y cloruro férrico en solución; dicho montaje se mantuvo ausente de luz natural. Los ensayos fueron realizados por un periodo de exposición a radiación de 6 horas una vez ajustado el pH inicial y dosificado el H2O2 y el FeCl3; el catalizador (Fe2+) fue aplicado en relación molar 1 a 10 con respecto a la dosis de peróxido de hidrógeno.
Considerando que uno de los principales contaminantes en las aguas residuales de pelambre es el sulfuro, el cual puede ser oxidado por el peróxido de hidrógeno a sulfato o azufre elemental dependiendo del pH de la solución (Tunay, Kabdasli, Arslan-Alaton, & Olmez-Hanci, 2010) dicho comportamiento se puede observar en las ecuaciones 1 y 2.
De acuerdo con las reacciones y con base en el rango de pH para el cual fueron realizados los ensayos, la oxidación realizada tiende a azufre elemental como producto, por otra parte y con el objeto de acelerar la reacción del peróxido de hidrógeno para formar radicales OH* responsables de la oxidación de sulfuros y materia orgánica, se empleó cloruro férrico como catalizador y radiación UV de modo que la reacción del peróxido en el agua (Rubio-Clemente, Chica & Peñuela, 2014) se representa conforme a las ecuaciones 3 y 4.
Resultados y discusión
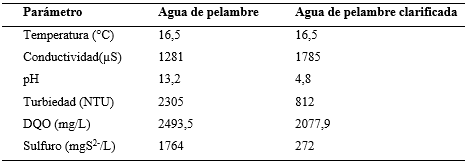
La caracterización del agua de pelambre cruda y el agua previamente clarificada, se presenta en la Tabla 1. Cabe señalar que para lograr la clarificación del agua residual se emplearon 1.5 g de sulfato de aluminio por cada litro de agua, hecho que dio como resultado la disminución del pH del agua residual y la volatilización de parte del sulfuro presente en el agua en forma de ácido sulfhídrico.
Tabla 1. Caracterización del agua residual antes y después de ser clarificada Fuente: autores, 2018.
Como resultado de la clarificación, también se observó la disminución de la concentración de sulfuros y DQO, debido a que gran parte del material sólido sedimentado es materia orgánica que puede retener una fracción de los sulfuros presentes en el agua de pelambre; además de la volatilización del sulfuro en forma de ácido sulfhídrico como fue previamente indicado, hecho que es ocasionado por el cambio del pH del agua a condiciones ácidas, lo que indica que la reacción de oxidación tomó lugar bajo las condiciones de la ecuación 1, es decir, se presenta una relación molar 1 a 1 entre el de H2O2 y el H2S.
A partir del diseño experimental y a través de la metodología propuestos, se determinaron los porcentajes de remoción para las variables estudiadas en cada uno de los ensayos realizados.
Tabla 2. Resultados de los ensayos del diseño experimental Fuente: autores, 2018.
Resultados de la anova
Los resultados obtenidos de la prueba estadística del análisis de varianza se evidencian en la tabla 3, tanto para la remoción de sulfuros como de DQO del agua residual y son expresados en los valores Fo y valor-p para evidenciar que tan significativos son los resultados obtenidos.
Tabla 3. ANOVA para el diseño experimental Fuente: autores, 2018.
Con respecto a los resultados del ANOVA, es claro que las variables de respuesta dependen o varían con respecto a las variables o factores de proceso, de ese modo, se rechaza la hipótesis nula. Por otra parte, se puede señalar que en el caso de la remoción de sulfuro el pH representa significancia estadística; sin embargo, con relación a la remoción de DQO, la dosis de H2O2 aplicada fue la variable o factor que presentó significancia estadística.
Efecto del pH y H2O2 sobre la remoción de sulfuros
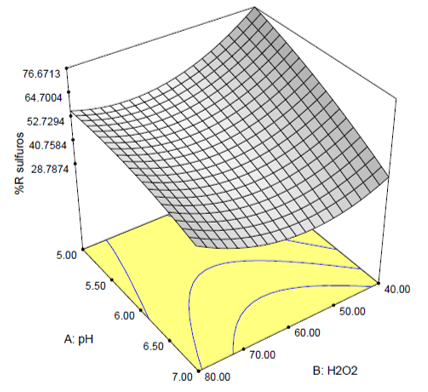
La figura 1 corresponde a la superficie de respuesta para la remoción de sulfuros con respecto al pH y dosis de H2O2, el coeficiente de correlación (R2) para esta superficie fue de 0.9084. la expresión matemática para la superficie de respuesta se presenta en la ecuación (5).
Figura 1. Superficie de respuesta para la remoción de sulfuros en función de las variable o factores de proceso. Fuente:autores, 2019.
A partir de la superficie de respuesta, se determina que dentro del rango de valores de los factores analizados, el porcentaje de remoción de sulfuros alcanza un valor máximo del 73,53%, para un pH inicial del agua igual a 5 y una dosis de peróxido de hidrógeno de 40 µg/L, es decir, para los valores más bajos de las variable o factores estudiados, lo cual concuerda con lo planteado en otras investigaciones en las cuales señalan que la oxidación por el proceso foto Fenton presenta mayores rendimientos a pH por debajo de 5 (Cruz-Rizo, Gutiérrez-Granados, Salazar & Peralta-Hernández, 2017). Para este caso se puede establecer que las condiciones de pH más bajas favorecen la remoción de sulfuros con una alta tasa de exposición a la luz visible.
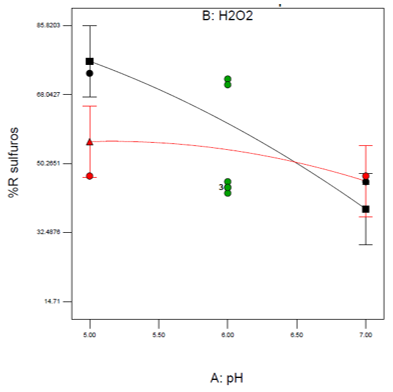
La figura 2 corresponde a la interacción de las variables y confirma que la variable que mayor influencia presenta sobre la remoción de sulfuros es el pH, tendencia que se mantiene hasta que el pH inicial de la solución es aproximadamente de 6.5, punto a partir del cual la dosis de H2O2 es la variable que mayor influencia presenta sobre la remoción de sulfuros.
Figura 2. Interacción de variables para la remoción de sulfuros. Fuente: autores, 2019.
Efecto del pH y H2O2 sobre la remoción de DQO
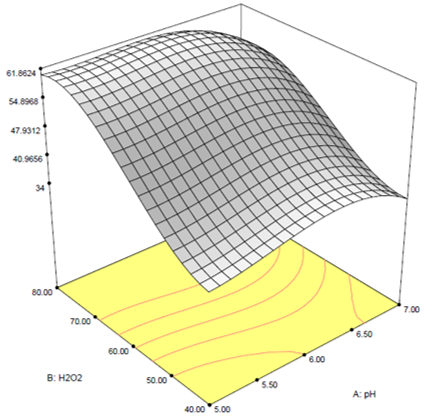
La figura 3 presenta la superficie de respuesta obtenida para describir la tendencia del porcentaje de remoción de DQO con respecto al pH inicial de la muestra y la dosis de H2O2, la ecuación que representa la superficie de respuesta corresponde a la ecuación 6.
Figura 3. Superficie de respuesta para la remoción de DQO en función de las variables o factores de proceso. Fuente: autores, 2019.
El coeficiente de correlación para la ecuación anterior presentó un valor de 0.7856, de ese modo no se logra una correlación favorable entre los datos experimentales y los pronosticados por el modelo matemático.
Con relación a la variable DQO, el máximo porcentaje de remoción alcanzado fue del 59%, pero en este caso, el pH inicial optimo fue 5 y la dosis de peróxido de hidrógeno fue la más alta dentro de los valores estudiados. La forma lineal de la gráfica permite señalar que no existe interacción entre las variables dosis de peróxido de hidrógeno y pH, es decir, para una misma dosis de H2O2, el porcentaje de remoción varía muy poco con respecto al pH, como se puede evidenciar en la Figura 4.
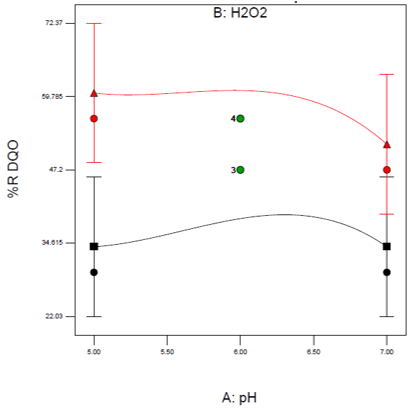
Figura 4. Interacción de variables para la degradación de DQO. Fuente: autores, 2019.
La figura de interacción permite señalar que la variable que mayor peso presenta sobre la remoción de DQO es la dosis de peróxido de hidrógeno, adicionalmente se puede establecer que las variables no interactúan, aunque se puede observar que a pH cercano a 6.5 la remoción de DQO presenta un valor mínimo para la dosis más baja de peróxido de hidrógeno, por su parte para la mayor dosis de agente oxidante la remoción disminuye ligeramente en la medida que el pH aumenta.
De acuerdo con los resultados, la dosis de peróxido de hidrógeno al 30 % requerida para lograr las máximas remociones alcanzadas en los ensayos debe ser de 1,6 L H2O2/m3 de agua clarificada con pH inicial de 5, el agua debe estar clarificada y ser expuesta a una fuente de radiación luz visible de 100 W.}
Análisis estequiométrico
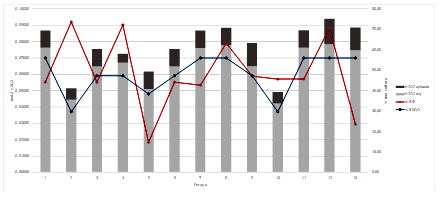
A partir de los valores de pH seleccionados para el diseño experimental, y de las ecuaciones 1 y 2 que determinan el comportamiento de reacción para los ensayos realizados, se establece la relación estequiométrica teórica, donde se obtienen la dosificación de H2O2 requerida para remover la concentración de sulfuros y de DQO iniciales, de igual manera se calcula por medio de la dosis de H2O2 aplicada, las moles de agente oxidante aplicado para comprender mejor la reacción de degradación que sucedió en el ensayo experimental. Como se observa en la figura 4, los resultados de remoción son bastante altos en comparación con la dosis de peróxido suministrada en cada ensayo, por ejemplo, dicha dosis representa solamente el 20,65% de la dosis total requerida según la naturaleza de reacción en el ensayo 5. Para los ensayos que mayor porcentaje de remoción presentaron se observa que, para la remoción de sulfuros alcanzada, la dosis de peróxido aplicada representa solamente el 15,85% del total requerido el 13.55 % para DQO.
Haga clic sobre la imagen para ampliarla
Figura 5. Dosis aplicada y requerida de H2O2 en relación con el porcentaje de remoción de sulfuros y de DQO. Fuente: autores, 2019.
Con este análisis se logra comprobar el efecto de la luz visible como promotor de radicales OH hecho que reduce el consumo del H2O2 requerido para la reacción de acuerdo con la reacción teórica. La combinación de peróxido de hidrógeno y radiación visible da lugar a un efecto sinérgico que intensifica la reacción para remover sulfuros y DQO. En otras palabras la acción oxidante del H2O2 se ve incrementada por la absorción de la luz visible para la oxidación de los contaminantes objeto de estudio.
Conclusiones
Se determinó que las variables de proceso o factores sí influyen sobre el porcentaje de remoción de sulfuros y DQO, de modo que la variable pH influye en mayor medida sobre la remoción de sulfuros por causa del equilibrio del H2S en solución acuosa.
Con base en los resultados de los ensayos se puede señalar que el mayor porcentaje de remoción de sulfuros se obtiene en condiciones ácidas, dentro del rango de pH inicial de solución entre 5 y 6. La máxima remoción de sulfuros fue del 73.53 % para un pH inicial de 5 y 40 µg/L de peróxido de hidrógeno, es decir, para los valores más bajos de los factores analizados.
Las dosis más altas de peróxido de hidrógeno dieron lugar a los mayores porcentajes de remoción de DQO, incluso mayores a los establecidos de acuerdo con la cantidad DQO removida, situación que se debe al efecto de la fotolisis por la radiación visible suministrada por lámparas LED. Se alcanzó un 59 % de remoción de DQO para pH inicial de 5 y 80 µg/L de dosis de peróxido de hidrógeno, indicando que la oxidación de la materia orgánica presente en el agua residual se ve favorecida por pH bajo y altas dosis de agente oxidante.
La presencia de hierro férrico favoreció la formación de radicales OH en el transcurso de la reacción, lo que permitió alcanzar un porcentaje de remoción tanto de sulfuros como de DQO superior al esperado por los cálculos estequiométricos.
Agradecimientos
Agradecemos a la Universidad Libre por permitir el desarrollo de esta investigación en los laboratorios de la Institución, además, a las curtiembres del municipio de Villapinzón que permitieron la toma de muestras de agua residual.
Potencial conflicto de interés
No existe posible conflicto de interés frente a la publicación de la presente investigación.
Fuentes de financiación
La financiación para lograr los objetivos propuestos de la presente investigación es de procedencia mixta, es decir, se tuvo la colaboración de la Universidad Libre bajo el departamento de Ingeniería ambiental de la Facultad de Ingenierías, asimismo, los autores financian parte de la investigación.
Referencias
Aboulhassan, M. A., Souabi, S. & Yaacoubi, A. (2008). Pollution reduction and biodegradability index improvement of tannery effluents. Int. J. Environ. Sci. Tech, 5(1), 11–16.
Andreozzi, R., Caprio, V., Insola, A. & Marotta, R. (1999). Advanced oxidation processes (AOP) for water purification and recovery. Catalysis Today, 53(1), 51–59. https://doi.org/10.1016/S0920-5861(99)00102-9.
APHA., AWWA & WPC. (1995). Standard Methods for the Examination of Water and Wastewater (20th Ed). Washington: AMERICAN PUBLIC HEALTH ASSOCIATION.
Artuz, L. A., Martínez, M. S. & Morales, C. J. (2011). Las industrias curtiembres y su incidencia en la contaminación del río Bogotá. Isocuanta, 1(1), 43–53. Retrieved from Link.
Bajza, E., Hitrec, P. & Muic, M. (2005). Influence of different concentrations of Al2(SO4)3 and anionic polyelectrolytes on tannery wastewater flocculation. Desalination, 171(1), 13–20. https://doi.org/10.1016/J.DESA1.2004.04.003.
Cruz-Rizo, A., Gutiérrez-Granados, S., Salazar, R. & Peralta-Hernández, J. M. (2017). Application of electro-Fenton/BDD process for treating tannery wastewaters with industrial dyes. Separation and Purification Technology, 172, 296–302. https://doi.org/10.1016/j.seppur.2016.08.029.
Cuartas-Uribe, B., Iborra-Clar, A., Bes-Piá, A., Mendoza-Roca, J. A., Galiana-Aleixandre, M. V. & Iborra-Clar, M. I. (2006). Nanofiltration of a simulated tannery wastewater: influence of chlorides concentration. Desalination, 191(1–3), 132–136. https://doi.org/10.1016/J.DESAL.2005.05.025.
Deghles, A. & Kurt, U. (2016). Treatment of tannery wastewater by a hybrid electrocoagulation/electrodialysis process. Chemical Engineering and Processing: Process Intensification, 104, 43–50. https://doi.org/10.1016/j.cep.2016.02.009.
Ganesh, R., Balaji, G. & Ramanujam, R. A. (2006). Biodegradation of tannery wastewater using sequencing batch reactor—Respirometric assessment. Bioresource Technology, 97(15), 1815–1821. https://doi.org/10.1016/J.BIORTECH.2005.09.003.
Gutiérrez-Pulido, H. & De la Vara Salazar, R. (2012). Análisis y diseño de experimentos. Recovered from https://doi.org/10.1017/CBO9781107415324.004.
Instituto de Hidrología, Meteorología, y Estudios Ambientales IDEAM. (2007). Toma de muestras de aguas residuales: instructivo para la toma de muestras de aguas residuales. Recuperado de: Link
Jian, S., Wenyi, T. & Wuyong, C. (2011). Kinetics of enzymatic unhairing by protease in leather industry. Journal of Cleaner Production, 19(4), 325–331. https://doi.org/10.1016/J.JCLEPRO.2010.10.011.
Nivya, T. K. & Pieus, T. M. (2016). Comparison of Photo ElectroFenton Process ( PEF ) and combination of PEF Process and Membrane Bioreactor in the treatment of Landfill Leachate. Procedia Technology, 24, 224–231. https://doi.org/10.1016/j.protcy.2016.05.030.
Rubio-Clemente, A., Chica, E. L. & Peñuela, G. A. (2014). Application of Fenton process for treating petrochemical. Wastewater, 16(2), 211–223. https://doi.org/10.1016/S1135-2523(12)60123- 3.
Saxena, S., Rajoriya, S., Saharan, V. K. & George, S. (2018). An advanced pretreatment strategy involving hydrodynamic and acoustic cavitation along with alum coagulation for the mineralization and biodegradability enhancement of tannery waste effluent. Ultrasonics Sonochemistry, 44, 299–309. https://doi.org/10.1016/j.ultsonch.2018.02.035.
Schrank, S. G., José, H. J., Moreira, R. F. P. M. & Schröder, H. F. (2005). Applicability of Fenton and H2O2/UV reactions in the treatment of tannery wastewaters. Chemosphere, 60(5), 644–655. https://doi.org/10.1016/j.chemosphere.2005.01.033.
Suthanthararajan, R., Ravindranath, E., Chits, K., Umamaheswari, B., Ramesh, T. & Rajamam, S. (2004). Membrane application for recovery and reuse of water from treated tannery wastewater. Desalination, 164(2), 151–156. https://doi.org/10.1016/S0011-9164(04)00174-2.
Tunay, O., Kabdasli, I., Arslan-Alaton, I., & Olmez-Hanci, T. (2010). Chemical Oxidation Applications for Industrial Wastewaters. Reino Unido.IWA.
Osorio Muñoz, L.C. (2014). Plan estratégico en las curtiembres de Villapinzón: competitividad e innovación en la cadena productiva del cuero “(Producción más limpia, asociatividad y desarrollo de alternativas de manejo y aprovechamiento de RS)”. Universidad Nacional de Colombia, Bogotá, Colombia.
Vilardi, G., Rodriguez-Rodriguez, J., Ochando Pulido, J. M., Verdone, N. & Di Palma, L. (2018). Pilot-Scale application of a real Tannery wastewater treatment by Fenton oxidation: Fe(II) and nZVI catalyst comparison and kinetic modelling. Process Safety and Environmental Protection, 117, 629–638. https://doi.org/10.1016/j.psep.2018.06.007.
1 Magíster en Ingeniería Ambiental. Universidad Libre. E-mail: This email address is being protected from spambots. You need JavaScript enabled to view it.. 2 Ingeniera Ambiental. Universidad Libre. E-mail: This email address is being protected from spambots. You need JavaScript enabled to view it.. 3 Ingeniero Ambiental. Universidad Libre. E-mail: This email address is being protected from spambots. You need JavaScript enabled to view it..
Para citar este artículo: Agudelo-Valencia, R. N., Ovalle-González, D. P. y Rodríguez-Rodríguez, L. F. (2020). Aplicación de foto denton (VIS) para la remoción de sulfuros y DQO en aguas residuales de curtiembre. Revista Luna Azul, 50, 215-228. Doi: DOI: 10.17151/luaz.2020.50.11
Esta obra está bajo una Licencia de Creative Commons Reconocimiento CC BY
|